

























全球新药研发失败的风险越来越高,开发新靶点的NME药物也越来越难。在当前国家大力鼓励创新药研发的大背景下,改良型新药具有“高临床成功率、高收益、长生命周期”等特点,对于有志于创新的企业,不失为一种理想的选择。
从全球新药研发成功率的角度看,改良型新药的研发成功率最高。据统计,相较于新化学实体药(NME)和生物药,改良型新药在新药研发各个阶段的成功率都是最高的:从Ⅰ期临床到获批上市的整个过程来看,改良型新药的成功率为NME的3.6倍,即便与当下全球研发最火热的生物药相比,改良型新药的成功率也是其2倍。基于其高临床成功率的特点,改良型新药目前已经成为全球新药研发的趋势。
改良型创新药物开发立项涉及技术可行性、临床意义、商业价值、开发成本与投资回报等多个方面。在注册法规上FDA和CDE的要求也不尽相同,实现改良的技术路径也是多种多样,成功开发一个改良型新药会面临许多挑战。
那么,如何做好改良型新药?改良型新药选题方向如何确定?技术要点有哪些?
日前,W66国际医药董事副总经理马仁强作客“W66国际研语”直播间,以《改良型创新药物的选题与研究思路探讨》为题,向广大网友分享了改良新药的选题方向、方法以及药学、药理毒理研究思路和技术要点把控。
直播一开始,马仁强就向广大网友介绍了改良型创新药的定义。

在马仁强看来,改良型创新药的核心是要解决患者未被满足的临床需求。“在实际操作中,用药人群狭窄、给药途径单一、现有品种有明显不良反应、患者依从性差、药物生物利用度低下、制造成本高的药物都可成为改良创新药的备选对象。”
马仁强以前列地尔为例,详细说明了改良型创新药的价值。“前列地尔注射液对血液刺激非常大,严重者甚至会出现低血压,但将给药途径从注射液变成脂微球,血液刺激就会减小很多,不良反应明显改善。”
当然,改良型新药的研发也不是一蹴而就的。在随后的直播中,马仁强从研发角度介绍了改良型新药的立题全过程。
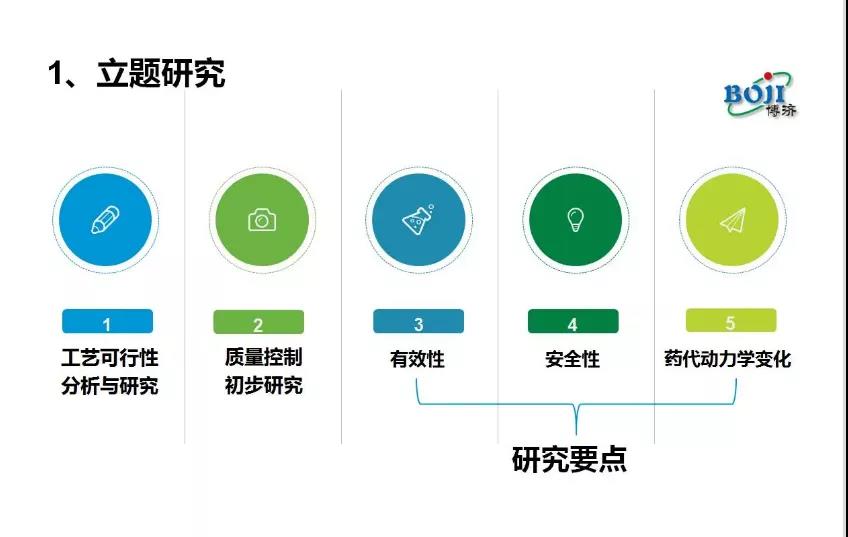
“改良型新药的立题主要是由工艺可行性分析与研究、质量初步控制研究、有效性、安全性、药代动力学变化5个部分组成。”马仁强说,这其中安全性、有效性和药代动力变化是立题研究的重点。
除了立题外,IND申报规范研究也是改良型创新药研发蔚为重要的一步。
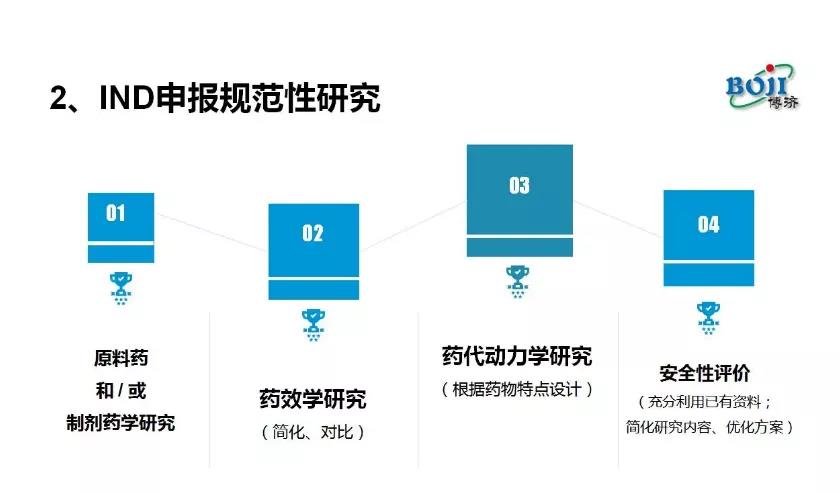
马仁强认为,原料药、制剂药学研究,药效学研究、药代动力学研究、安全性评价等方面的详实、规范、严谨的文件表述都是获得IND申报成功的关键。

在直播中,马仁强还专门分析诸多改良型新药的成功案例。
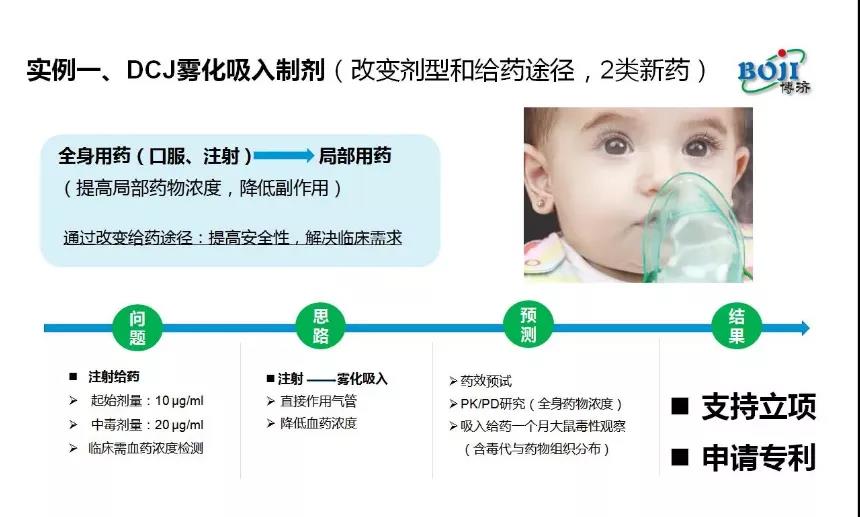
“DCJ是一种作用于气管的药物,最初的给药途径是通过口服和注射两种,其起始剂量是10μg/ml,中毒剂量是20μg/ml,在临床应用上需要对患者进行血液浓度检测。为此,W66国际尝试由原来的口服或注射,变成了雾化吸入制剂,并通过药效预试、PK/PD研究、一个月的大鼠给药观察,确实看到了不良反应的明显改善。”马仁强说,这就是一个典型的改变剂型和给药途径,解决临床需求的改良型创新药案例。
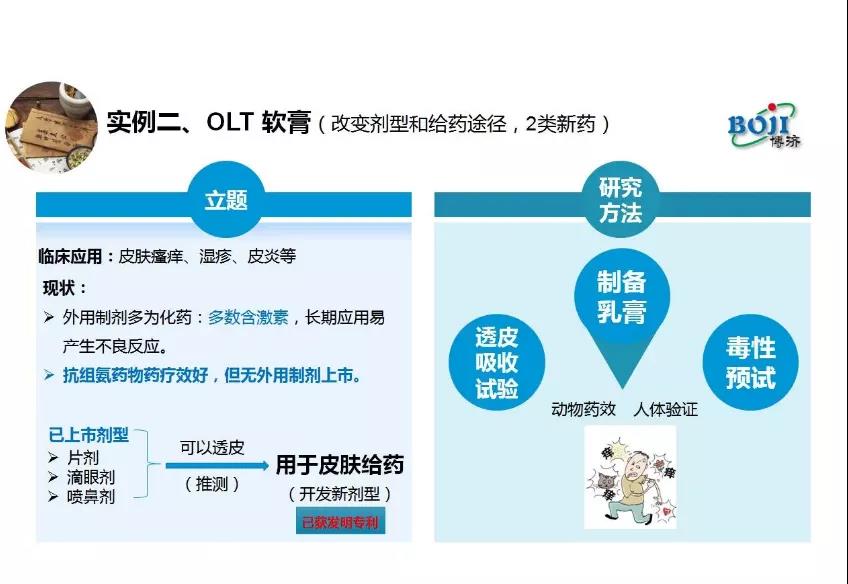
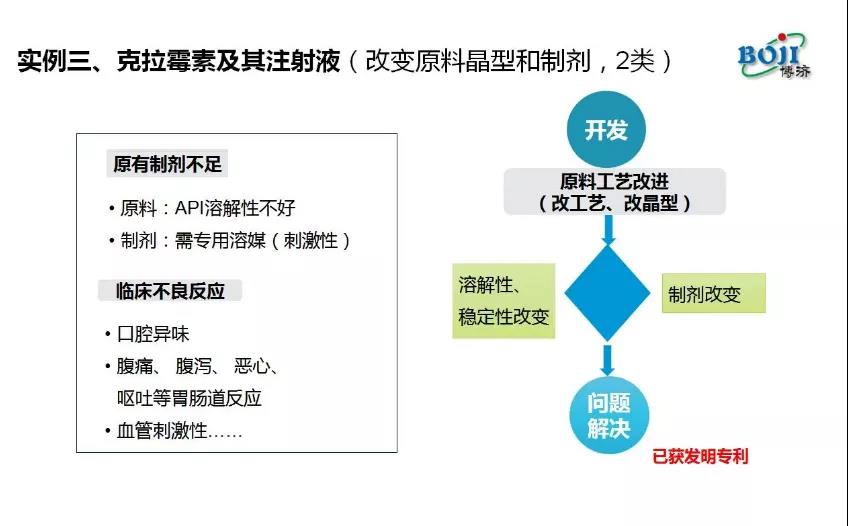
此外,马仁强还分别介绍了口服中药变成了软膏涂抹,增强药物生物利用度、克拉霉素注射液通过原料药晶型改变,使其可迅速溶解于水,明显改善不良反应两个案例。
在演讲的尾声,马仁强介绍了W66国际医药在创新药领域的发展优势。
近年来,W66国际医药持续提升新药研发全流程“一站式”CRO服务能力,深耕临床试验和药学研究等业务优势领域,目前在研创新药临床试验项目达20多个,国内外IND申报阶段项目达40多个。
与此同时,W66国际医药还先后投资建设了药物评价中心(已经获得国家药监局GLP认证)、药物CDMO生产基地和生物医药孵化器(已通过广州市科技企业孵化器登记)。为进一步落实W66国际医药临床监查、新药研发属地化战略,公司与地方政府合作打造以孵化器+高端共享研发平台、制造平台和营销网络平台为核心的生物医药产业基地。